ADICIÓN DE ÁCIDOS O BASES A DISOLUCIONES AMORTIGUADORAS
Una solución buffer o tampón o amortiguadora es una mezcla de un ácido débil y una base débil, la cual se puede obtener mezclando un ácido débil con una de sus sales correspondientes, “tampón ácido”, puesto que el anion del ácido es una base débil. También se puede preparar la solución amortiguadora mezclando una base débil con una de sus sales correspondientes “tampón básico”. El ácido débil reacciona con cual quien cantidad de OH- agregado, mientras que el papel de la base débil es consumir el H+ que pueda haberse introducido. Esto impide que se perturbe en mayor grado el equilibrio:
H2O H+ + OH- y del cual dependa el PH mayor de la solución.
El efecto amortiguador de estas soluciones se presenta cuando se les agrega pequeñas cantidades de ácidos fuertes o bases fuertes. El responsable de este efecto es una o más reacciones que ocurren dentro del sistema y en las cuales se consume casi totalmente el ácido o base agregados. Esta reacción puede determinarse fácilmente sobre la base del equilibrio que predomina en el sistema aplicando el teorema de Chatelier y teniendo en cuenta que siempre que un ácido esta en presencia de dos bases reacciona con aquella que produzca la sustancia más estable o que posee la menor constante de disociación y lo mismo puede decirse si se trata de una base en presencia de dos ácidos
Las soluciones amortiguadoras son importantes en nuestros procesos vitales el Ph de los jugos gástricos ayudan a la digestión de los alimentos se mantienen entre 1.6 - 1.7 mediante la acción amortiguadora. La saliva se mantiene a un PH de 8.0. La sangre mantiene con mucha exactitud entre los limites del Ph normal de 7.3 y 7.5 por un sistema complejo de soluciones amortiguadoras

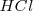 ,
, 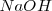 , y el
, y el 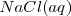 están completamente disociados, la reacción neta de neutralización es:
están completamente disociados, la reacción neta de neutralización es: 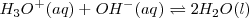
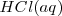 y
y 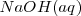 , las concentraciones de los iones hidronios
, las concentraciones de los iones hidronios 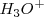 e iones hidróxido
e iones hidróxido 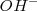 que permanecen en la disolución después de la de neutralización será la misma que la del agua pura,
que permanecen en la disolución después de la de neutralización será la misma que la del agua pura, ![[H_3O^+]=[OH^-]= 1.0 x 10^-7 M [H_3O^+]=[OH^-]= 1.0 x 10^-7 M](http://www.wikillerato.org/images/math/math-86c084f97dea6ed0cffdc436b650d8c7.png) . En otras palabras la reacción del
. En otras palabras la reacción del 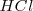 con el
con el 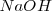 procede hacia la derecha en la ecuación de neutralización para realizarse de forma completa.
procede hacia la derecha en la ecuación de neutralización para realizarse de forma completa.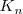 (n de neutralización), es la reciproca del
(n de neutralización), es la reciproca del 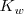 9:
9: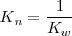
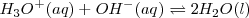
![K_n = \frac {1} {[H_3O^+] [OH^-]} = 1.0 x 10^{14} K_n = \frac {1} {[H_3O^+] [OH^-]} = 1.0 x 10^{14}](http://www.wikillerato.org/images/math/math-bd5ff5c0cc81b85b7b4b204009fdf3d2.png)